|
| Fluxul de Stiri dupa Data Aparitiei |
|
Comentarii Adauga Comentariu _ Echipa descoperă un mecanism care protejează țesutul după o expresie defectuoasă a genelor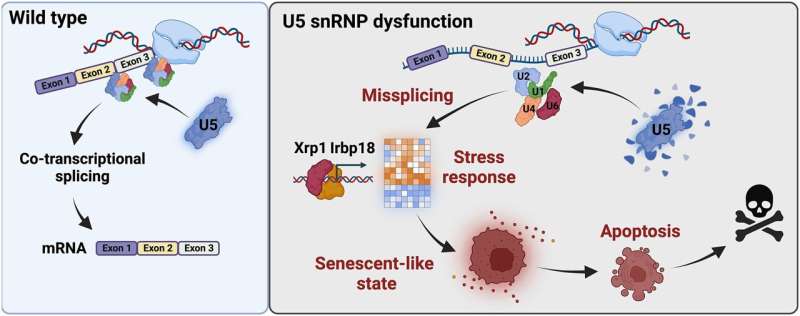 _ Echipa descoperă un mecanism care protejează țesutul după o expresie defectuoasă a genelorUn studiu efectuat la Universitatea din Köln, Cluster-ul CECAD de excelență în cercetarea îmbătrânirii, a identificat un complex de proteine care este activat de defecte ale spliceozomului, foarfecele moleculare care procesează informațiile genetice. Cercetările viitoare ar putea duce la noi abordări terapeutice pentru tratarea bolilor cauzate de splicing defectuos. Materialul genetic, sub formă de ADN, conține informațiile care sunt esențiale pentru funcționarea corectă a fiecărei celule umane și animale. Din acest depozit de informații se generează ARN, un intermediar între ADN și proteină, unitatea funcțională a celulei. În timpul acestui proces, informațiile genetice trebuie adaptate pentru funcțiile specifice ale celulei. Informațiile care nu sunt necesare (intronii) sunt tăiate din ARN și componentele importante pentru proteine (exoni) sunt păstrate. O echipă de cercetători condusă de profesorul dr. Mirka Uhlirova de la CECAD de la Universitatea din Köln Grupul de excelență în cercetarea îmbătrânirii a descoperit acum că, dacă procesarea acestor informații nu mai funcționează corect, un complex proteic (heterodimer C/EBP) este activat și direcționează celula către o stare latentă, cunoscută sub numele de senescență celulară. Rezultatele apar sub titlul „Xrp1 guvernează programul de răspuns la stres la disfuncția spliceosome” în Nucleic Acids Research. Toate eucariotele (adică organismele în care ADN-ul este închis în nucleul celulei) au un spliceosome. Aceasta este o mașină care efectuează „splicing”, îndepărtarea intronilor și legarea exonilor pentru a forma ARN mesager (ARNm). Defecțiunile spliceozomului duc la boli cunoscute sub denumirea de spliceosomopatii, care pot afecta multe țesuturi diferite și se manifestă ca degenerare a retinei sau sindrom mielodisplazic, un grup de boli ale măduvei osoase care afectează sângele. În studiu, Uhlirova Laboratorul a folosit modelul de organism Drosophila melanogaster, o muscă de fructe, pentru a investiga modul în care celulele dintr-un organism în curs de dezvoltare răspund la defecțiunea spliceosome. Oamenii de știință au folosit o combinație de genomică și genetică funcțională pentru a determina rolul genelor individuale și interacțiunile dintre ele. Studiul a arătat că celulele care suferă de o snRNP spliceosomal U5 (particulă mică de ribonucleoproteină nucleară U5) activează o răspunsul de semnalizare a stresului și comportamentele celulare care sunt caracteristice senescenței celulare. Programul de senescență modifică funcțiile cruciale ale celulelor. Împiedică divizarea celulelor în timp ce le stimulează secreția. Senescența este declanșată pentru a păstra celulele care sunt deteriorate, deoarece eliminarea lor imediată ar provoca mai mult rău decât bine. Cu toate acestea, acumularea de celule senescente poate avea un impact negativ asupra unui țesut, precum și asupra întregului organism. Prin urmare, aceste celule sunt în cele din urmă eliminate. Echipa lui Uhlirova a identificat complexul proteic C/EBP-heterodimer, Xrp1/Irbp18, drept motorul critic al programului de răspuns la stres cauzat de îmbinarea defectuoasă. Reglarea Xrp1/Irbp18 în celulele deteriorate a dus la creșterea producției de proteine și a indus o stare asemănătoare senescenței. „Senescența este o sabie cu două tăișuri”, a spus Uhlirova. Un avantaj al celulelor senescente este că nu sunt toate eliminate prin moartea celulelor în același timp, menținând astfel integritatea țesutului. La urma urmei, țesutul parțial intact este mai bun decât deloc. Cu toate acestea, aceste celule creează probleme pe termen lung, deoarece acumularea lor promovează boala și îmbătrânirea. „Un spliceosome funcțional este o condiție prealabilă de bază pentru celulele, țesutul și întregul organism sănătos”, a concluzionat ea. „O investigație suplimentară a programului de semnalizare a stresului pe care l-am identificat va fi importantă pentru a despacheta în continuare răspunsurile complexe declanșate de defecte ale mașinilor esențiale care controlează expresia genelor și cum le putem influența”. În viitor, rezultatele ar putea contribui la dezvoltarea unor abordări terapeutice pentru tratarea bolilor cauzate de disfuncționalități ale spliceozomului.
Linkul direct catre PetitieCitiți și cele mai căutate articole de pe Fluierul:
|
|
|
Comentarii:
Adauga Comentariu